Her ne kadar birbirinden ayrı gibi düşünülse de tıpta, elektrik alan kullanımının birçok örneğini günümüzde görmekteyiz. Özellikle son yıllarda, araştırmacılar, elektrik alanın hangi alanlarda kullanabileceğini ve etkinliği üzerine yoğunlaştılar. Elde edilen verilere göre, genetik mühendisliğinden kansere ve hatta yara iyileşmesine kadar birçok alanda elektrik alandan faydalanmak oldukça etkili sonuçlar veriyor.
Yazan: Sedef Çakır
Her ne kadar birbirinden ayrı gibi düşünülse de, tıpta elektrik alan kullanımının birçok örneğini günümüzde görmekteyiz. Özellikle son yıllarda, araştırmacılar, elektrik alanın hangi alanlarda kullanabileceğini ve etkinliği üzerine yoğunlaştılar. Elde edilen verilere göre, genetik mühendisliğinden kansere ve hatta yara iyileşmesine kadar birçok alanda elektrik alandan faydalanmak oldukça etkili sonuçlar veriyor.
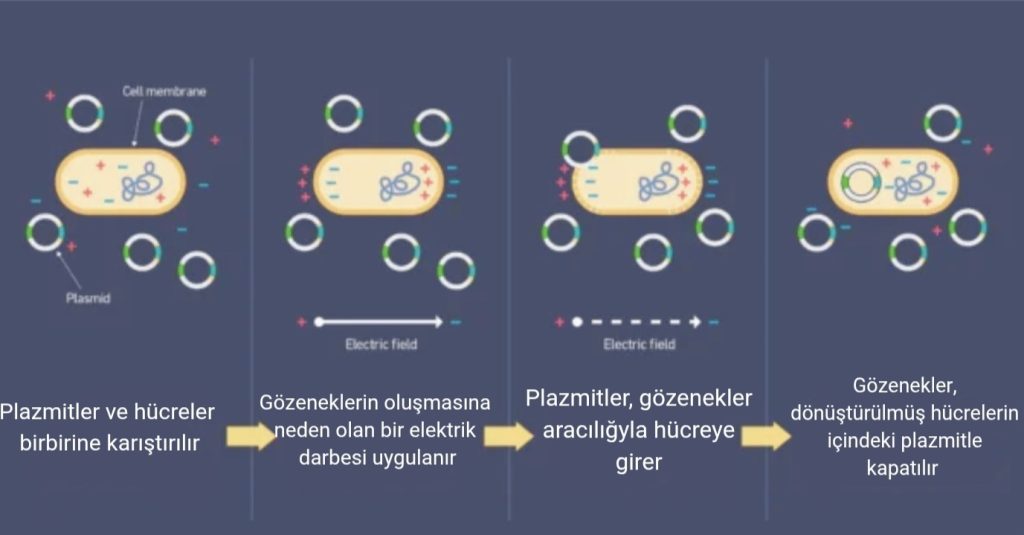
Elektroporasyonda hücre zarına kısa süreli elektrik impulsları uygulanır. Böylece, hücre zarı geçici olarak geçirgen hale gelir.
Tıpta elektrik alanın uygulandığı çeşitli yöntemler bulunmaktadır. Bunlardan birisi de elektroporasyon yöntemidir. Elektroporasyonda hücre zarına kısa süreli elektrik impulsları uygulanır. Böylece, hücre zarı geçici olarak geçirgen hale gelir. Bu sayede, normalde hücre içine giremeyen moleküller zardan kolayca geçebilir. Şüphesiz ki, bu uygulamanın kanser tedavilerinden kozmetik sektöründeki uygulamalara kadar pek çok alanda çok büyük yararları vardır. Elektroporasyon yönteminin etkinliğinin uygulanan voltaj, elektrik darbesinin süresi ve darbe sayısı gibi parametrelerden etkilendiği de unutulmamalıdır. Bütün bu parametrelere dikkat edilmesi ile tedavi etkinliği arasında doğrudan bir ilişki vardır.
Elektroporasyon çeşitleri
IRE (Geri Dönüşümsüz Elektroporasyon): Hücre ölümünü tetiklemek için kullanılan bir yöntemdir. Burada 1.5–3 kV aralığında, 80–100 mikrosaniyelik, 60–100 adet yüksek voltajlı elektrik darbeleri uygulanarak iyon dengesi bozulur ve kalsiyum aşırı yüklenmesi sebebiyle hücrede oldukça toksik olan yüksek seviyede reaktif oksijen türleri (ROS) aktive olur ve dolayısıyla ozmotik hücre ölümü gerçekleşir.
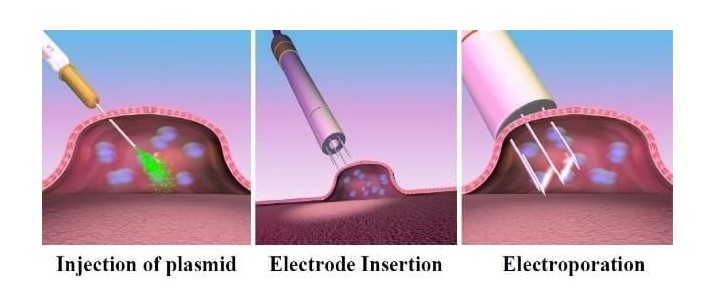
Gen elektrotransferi (GET): Hedeflenen hücrenin zarında gözenek oluşumuna sebep olarak plazmidler gibi genetik parçaların hücre içine alınmasını kolaylaştırır. Elektrik alanın hücre zarında geçici porlar oluşturmasıyla DNA hücre içine girer ve burada gen ekspresyonu başlar. DNA aşıları, kanser immünoterapisi, gen tedavisi, kas hastalıkları ve cilt hastalıkları gibi alanlarda kullanılır. Bu teknolojiden günümüzde birçok genetik mühendisi yararlanır.
Kalsiyum elektroporasyonu (Ca–EP): Mekanizmasında yüksek voltajlı elektrik darbelerinin hücre zarında geçici geçirgenlik oluşturmasıyla tümör hücrelerine yüksek miktarda kalsiyum iyonu elektroporasyon yoluyla aktarılır. Kalsiyum, reaktif oksijen türlerinin (ROS) aktivasyonu gibi birçok süreçte kilit bir rol oynar. Kalsiyum elektroporasyonu sayesinde, hücre içindeki kalsiyum miktarının artışı, hücresel stres oluşturarak hücrede enerji (ATP) tükenmesine neden olabilir. Bu durum da kanser hücrelerinin ölümünü tetikler.
EP–TVL (Elektroporasyon Tabanlı Terapötik Vezikül Yüklemesi): Oldukça yenilikçi bir uygulamadır. Elektroporasyon, kemoterapi ajanları, toksinler, antikorlar ve bitki kökenli moleküller gibi anti-kanser özelliklere sahip çeşitli ajanlarla nano veziküllerin (lipozomlar, eksozomlar) yüklenmesine olanak tanır. Böylece, bu ajanların hücre zarından geçişi daha kolay hâle gelir ve tümör karşıtı etkinlikleri artırılır.
Elektrokemoterapi (ECT): Kanser tedavisinde kemoterapi ilaçlarının enjeksiyonu için sıklıkla tercih edilen bir yöntemdir. Bu yöntemde, tümör dokularına elektrik akımı uygulanır. Böylece, tümör hücre zarı gerçirgen hale gelerek bleomisin ve sisplatin gibi ilaçların hücre içine alınmasını sağlar. Bu elektroporasyon çeşidi sayesinde, kemoterapi dozları ve yan etkileri azaltılarak ilaçların etkinliği artırılır. Sonuç olarak, kanserli hücre ölümü tetiklenmiş olur.
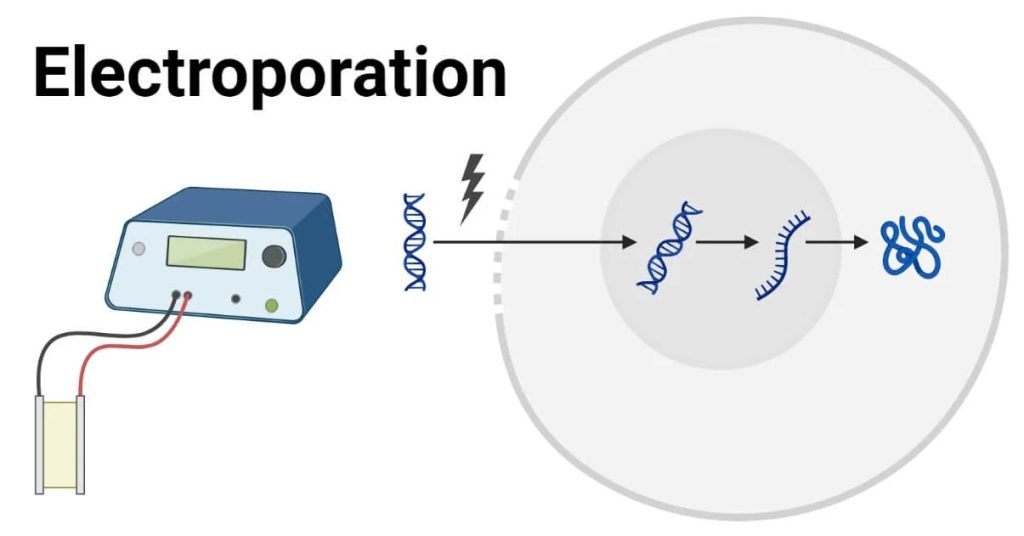
Elektroporasyonun çalışma mekanizması
Hücreler elektrik alan altındayken zar boyunca bir transmembran potansiyeli oluşur. Bunun sonucunda, hücre zarında bir yük birikimi oluşur. Elektrik alan, hücre zarındaki moleküllerin hizalanmaları için onları zorlar. Elektrik alana maruz kalan transmembran potansiyeli belirli bir limiti aştığında hücre geçici olarak geçirgen hale gelir ve zar üzerinde gözenekler oluşur. Elektrik alan uygulama süresi arttıkça dengesizleşmiş zar ve oluşan gözenekler daha stabil bir hal alır ve zamanla daha büyük gözenekler oluşur. Normalde hücre içine giremeyen DNA gibi büyük moleküller, bu sayede hücreye geçiş yapabilirler.
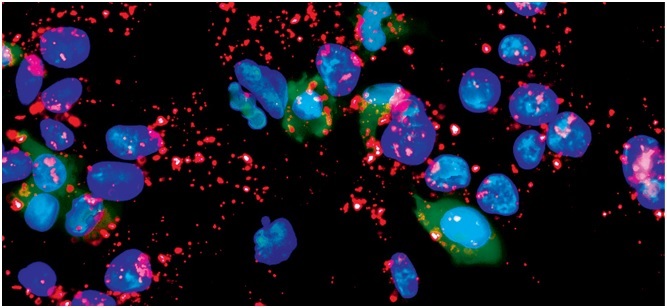
DNA’nın sitoplazmaya girdikten sonra ifade edilebilmesi için hücre çekirdeğine ulaşması gerekir; çünkü gen ekspresyonunun ilk aşaması olan transkripsiyon hücre çekirdeğinde gerçekleşir. Yapılan çalışmalar, plazmidlerin hücre çekirdeğine gitmek için sitoplazmadaki mikrotübül ağını ve proteinleri kullandığını ortaya koymuştur.
Elektroporasyon ve kanser
Günümüzde, kanser tedavilerinde elektroporasyon yönteminden sıklıkla yararlanılmaktadır. IRE, ECT ve Ca-EP gibi yöntemlerle hücrede hücre zarının geçirgenleştirilmesiyle kanserli hücrelerin ölümü tetiklenebilir. Aynı zamanda, hücreye kemoterapi ilaçları verilerek hedefe yönelik tedaviler sağlanabilir. Geri dönüşümsüz elektroporasyon (IRE) evcil hayvanlar üzerinde de araştırılmaktadır. Hatta, yapılan bir çalışmada, glioma (beyin tümörü) tanısı almış altı köpek IRE ile tedavi edilmiştir.
Ayrıca, günümüzde elektrokemoterapi (ECT) yöntemi de yine evcil hayvanlarda uygulandığında oldukça iyi sonuçlar vermiştir. Örneğin, karsinom ve melanoma tedavisinde, ECT uygulanan hayvanlarda, tedavi başarısı sağlanmıştır. İnsanlar üzerinde de onlarca kanser türü üzerindeki klinik araştırmalar devam etmektedir ve şu zamana kadar elde edilen sonuçlar oldukça umut vericidir. Kalsiyum elektroporasyonu ve diğer tüm elektroporasyon çeşitlerinde de kanser çalışmaları üzerine araştırmalar sıkı bir şekilde sürdürülmektedir. Eski yöntemlerin aksine, geliştirilen bu yöntemler hem daha hızlı hem de çok daha efektif bir şekilde çalıştığından, tedavi başarısı da yüksektir. Ayrıca, bu yöntemler sayesinde, doz ayarı yapılabilir ve yan etkiler azaltılabilir.
İnsanlar üzerinde de onlarca kanser türü üzerindeki klinik araştırmalar devam etmektedir ve şu zamana kadar elde edilen sonuçlar oldukça umut vericidir.
Genetik ve elektroporasyon
Genetik mühendisliği alanında gen transferi olmazsa olmaz uygulamalardan birisidir. Gen terapisinde viral ve viral olmayan (non-viral) yöntemler kullanılır. Viral vektörler verimlilik açısından ciddi avantajlar sunar. Fakat, yüksek maliyet, sitotoksisite (hücrelere zarar verme potansiyeli), mutagenez (genetik mutasyonlara yol açma) riski ve aktarılabilecek gen boyutunda sınırlama gibi bazı dezavantajları da bulunmaktadır. Diğer bir yandan, plazmidler gibi non-viral vektörler, çok daha düşük maliyetli olduğundan ve daha güvenli olduğundan dolayı tercih edilebilir. Fakat, bütün bu sağladığı avantajlara karşın, çok daha düşük düzeyde gen aktarımı ve gen ekspresyonu sağlar. Verimliliği düşük olduğu için çalışmaların başarısızlıkla sonuçlanmasına sebebiyet verebilir. Yapılan çalışmalar, bunun gibi karışık durumlarda kas dokusunda gen ekspresyonunun elektrik alan uygulamasıyla önemli ölçüde arttığını göstermiştir. Elektroporasyon yöntemi sayesinde, güvenli ve yüksek düzeyde gen aktarımı yapılabilir.
Elektroporasyon CRISPR yöntemi uygulanırken gen düzenleme malzemelerini hücre içine aktarmak için de kullanılabilir.
Gen aktarımında elektroporasyon elektrik alan parametreleri, elektrot tasarımı, hedeflenen hücreler ve aktarılmak istenen plazmidler gibi faktörlerden ciddi şekilde etkilenir. Burada diğer bir göz önünde bulundurulması gereken nokta ise, sürecin etkili olması için tek bir kombinasyonun olmadığıdır. Hedeflenen sonuç için gerektiğinde optimizasyon yapılması başarı oranını ciddi bir şekilde artırır. Genetik alanında elektroporasyon gen aktarımı, aşı üretimi, transgen ekspresyonu ve enzim tedavisinde oldukça başarılı bir etki gösterir. Ayrıca, CRISPR/cas9 teknolojisi burada da karşımıza çıkmaktadır. Elektroporasyon CRISPR yöntemi uygulanırken gen düzenleme malzemelerini hücre içine aktarmak için de kullanılabilir. Bazı durumlarda nanometre boyutunda küçük porlar açılması gerekir. Bunun için “nanoelektroporasyon” adı verilen yöntem kullanılır. Burada hücre zarı çok daha küçük ölçekli ve hassas bir şekilde delinir. Nanoteknolojinin hızla geliştiği günümüzde bu yöntem de genetik mühendisleri tarafından sıklıkla tercih edilir.
Cilt yapısı ve transdermal ilaç taşıma sistemleri
Cildimiz, vücudumuzdaki en büyük organdır. Cildimizin diğer organlarımız gibi pek çok hayati fonksiyonu bulunur. Zararlı maddeler ve mikroplar gibi tehditlere karşı koruyucu bariyer oluşturma, vücudumuz için çok önemli olan suyun aşırı kaybını önleme, UV ışınlarına karşı bizi koruma, vücutta homeostazı (vücudun iç dengesi) sürdürme ve ciltte bulunan özel reseptörler sayesinde basınç, ağrı ve sıcaklık değişimleri gibi çevresel etkilere yanıt verme gibi özellikler, derimizi tüm vücut sağlığımız için çok önemli bir yere koyar.
Cildimiz, vücudumuzdaki en büyük organdır. Cildimizin diğer organlarımız gibi pek çok hayati fonksiyonu bulunur.
Yapısal özelliklerine bakıldığında, derimiz çeşitli katmanlardan meydana gelir. Bu katmanların kalınlığı ve bileşimi vücuttaki farklı lokasyonlarda farklılık gösterebilir. Keratinositlerin (cilt hücreleri) şekli, yapısı ve farklılaşma düzeyleri katmanlar arasında bazı değişikliklere sebep olabilir. Derinin en dış tabakası olan epidermis, keratinositler ve dendritik hücreler gibi bağışıklık sistemi hücrelerinden oluşur. Dendritik hücreler sayesinde, vücut zararlı dış etkenlerden kendini korur. Ayrıca, melanositler melanin pigmenti üreterek cilt rengini oluşturur. Derinin bir alt katmanı olan dermis, epidermisin altında konumlanır. Kan damarları, sinir uçları, kıl kökleri, ter ve yağ bezleri dermiste bulunur. Ayrıca, kolajen sentezleyen fibroblastlar, makrofajlar ve mast hücreleri gibi pek çok bağışıklık hücresi de yine bu tabakada bulunur. Kolajen ve elastin lifler ise deriye esneklik ve dayanıklılık sağlar.
Hipodermis (Subkutan Doku) ise en alt katmandır. İçerisindeki yağ dokusu ile vücudu ısı ve darbelere karşı korur. Bu yağ dokusu aynı zamanda enerji kaynağı olarak da kullanılır. Transdermal ilaç taşıma sistemleri (TDDS), enjeksiyon yapılmadan sağlıklı cilde doğrudan uygulanır ve ağrısız olmasından kaynaklı hastalar ve doktorlar tarafından sıklıkla tercih edilir. TDDS, ilaçları kontrollü bir hızda uygular. Bu sayede, sürekli ve sabit ilaç salınımını destekler. Dolayısıyla, ortaya çıkabilecek yan etkiler minimize edilir. TDDS, daha düşük ve kontrollü ilaç düzeyleri uygulayarak, biyoyararlanımı artırır ve tedavide daha iyi sonuçlar alınmasına imkan sağlar. IP ve EP gibi elektrikle desteklenen iletim teknikleri, deri rahatsızlıkları için oldukça etkilidir.
Transdermal ilaç taşıma sistemleri (TDDS), enjeksiyon yapılmadan sağlıklı cilde doğrudan uygulanır ve ağrısız olmasından kaynaklı hastalar ve doktorlar tarafından sıklıkla tercih edilir.
İnvazif olmayan bir ilaç taşıma yöntemi olan iyontoforez (IP), düşük yoğunluklu elektrik akımı kullanarak yüklü moleküllerin cilt altına taşınmasına olanak tanır. Non- invazif olan bu yöntem, enjeksiyon yapılmadan uygulanır. Diğer bir yöntem olan EP (elektroporasyon) ise, ciltte geçici porlar açarak transdermal ilaç iletimini artırır. Fakat, IP’den farklı olarak EP, ağrı ve kas kasılmaları gibi yan etkilere neden olabilir. Bu yöntemlere ek olarak, mikroiğnelerin (MN) iyontoforez (IP) ve elektroporasyon (EP) ile entegrasyonu gerçekten tatmin edici sonuçlar sunabilir. MN’ler, ciltte düşük dirençli sulu geçitler oluşturarak, IP veya EP’nin bu geçitleri kullanarak ilaç akışını artırmasına olanak tanır.
Elektrik, yaraları nasıl üç kat daha hızlı iyileştirebilir?
Diyabet hastaları ve yaşlılar kronik yaralar sonucu ciddi acılar çekmekte ve bu yaraları iyileştirmek için çeşitli yöntemler aramaktadır. İsveç’teki Chalmers Teknoloji Üniversitesi ve Almanya’daki Freiburg Üniversitesi’nde yürütülen bir projede, araştırmacılar, elektrik kullanarak yara iyileşmesini hızlandıran ve yaraların üç kat daha hızlı iyileşmesine olanak tanıyan bir yöntem geliştirdiler. Araştırmacılar, bu yöntemi geliştirirken, yaralı cildin elektrik uyarımıyla iyileştirilebileceği yönündeki eski bir hipotezden ilham aldılar. Bu fikir, cilt hücrelerinin elektrotaktik olduğuna, yani elektrik alanları doğrultusunda “göç ettiklerine” dayanıyor.
Araştırmacılar, bir biyoçip geliştirdiler. Hücrelere küçük yaralar açtılar ve bu yaralardan bazılarını elektrik akımıyla uyardılar. Bu yaralar, elektriksel uyarım almayan yaralara kıyasla üç kat daha hızlı iyileşti.
Bu da, bir petri kabına cilt hücreleri yerleştirilip bir elektrik alan uygulandığında hücrelerin rastgele değil, aynı yöne doğru hareket ettikleri anlamına geliyor. Araştırmacılar, bir biyoçip geliştirdiler. Hücrelere küçük yaralar açtılar ve bu yaralardan bazılarını elektrik akımıyla uyardılar. Bu yaralar, elektriksel uyarım almayan yaralara kıyasla üç kat daha hızlı iyileşti. Ekip, aynı zamanda diyabet sonucu oluşan yaralara da odaklandı. Hücrelerde diyabet taklit edildiğinde çip üzerindeki yaralar çok yavaş şekilde iyileşti. Fakat, elektriksel uyarım uygulandığında iyileşme ciddi şekilde arttı ve diyabetten etkilenen hücreler sağlıklı cilt hücreleri haline geldi.
Kaynakça
Electroporation in Translational Medicine: From Veterinary Experience to Human Oncology – PMC
Electroporation-Mediated Gene Delivery – PMC
(PDF) ELEKTROPORASYON VE KLİNİK UYGULAMARI
Iontophoresis and electroporation-assisted microneedles: advancements and therapeutic potentials in transdermal drug delivery | Drug Delivery and Translational Research
How electricity can heal wounds three times as fast | EurekAlert!